製品基本Q&A
製品基本Q&A
アトーゼット®(エゼチミブ/アトルバスタチンカルシウム水和物)
製品情報
効能又は効果は?
高コレステロール血症、家族性高コレステロール血症です。
<効能又は効果に関連する注意>
本剤を高コレステロール血症、家族性高コレステロール血症の治療の第一選択薬として用いないでください。
適用の前に十分な検査を実施し、高コレステロール血症、家族性高コレステロール血症であることを確認した上で本剤の適用を考慮してください。
ホモ接合体性家族性高コレステロール血症については、LDLアフェレーシス等の非薬物療法の補助として、あるいはそれらの治療法が実施不能な場合に本剤の適用を考慮してください。
<引用>
添付文書
<効能又は効果に関連する注意>
本剤を高コレステロール血症、家族性高コレステロール血症の治療の第一選択薬として用いないでください。
適用の前に十分な検査を実施し、高コレステロール血症、家族性高コレステロール血症であることを確認した上で本剤の適用を考慮してください。
ホモ接合体性家族性高コレステロール血症については、LDLアフェレーシス等の非薬物療法の補助として、あるいはそれらの治療法が実施不能な場合に本剤の適用を考慮してください。
<引用>
添付文書
作用機序は?
小腸でのコレステロール及び植物ステロールの吸収を選択的に阻害するエゼチミブと、コレステロールの生合成を阻害するアトルバスタチンの配合剤です。
アトルバスタチンは肝臓のHMG-CoA還元酵素を選択的かつ競合的に阻害し、肝臓のコレステロール合成を抑制します。
エゼチミブは小腸壁細胞に存在する蛋白質(Niemann-Pick C1 Like 1)を介してコレステロール及び植物ステロールの吸収を阻害します。その結果、肝臓のコレステロール含量が低下し、肝臓でのコレステロールの生合成が代償的に亢進します。
アトーゼット®配合錠は、1剤でコレステロールの肝臓での合成と小腸での吸収を阻害する作用を有します。
<引用>
添付文書
アトルバスタチンは肝臓のHMG-CoA還元酵素を選択的かつ競合的に阻害し、肝臓のコレステロール合成を抑制します。
エゼチミブは小腸壁細胞に存在する蛋白質(Niemann-Pick C1 Like 1)を介してコレステロール及び植物ステロールの吸収を阻害します。その結果、肝臓のコレステロール含量が低下し、肝臓でのコレステロールの生合成が代償的に亢進します。
アトーゼット®配合錠は、1剤でコレステロールの肝臓での合成と小腸での吸収を阻害する作用を有します。
<引用>
添付文書
使用方法
用法及び用量は?
通常、成人には1日1回1錠(エゼチミブ/アトルバスタチンとして10mg/10mg又は10mg/20mg)を食後に経口投与します。
<用法及び用量に関連する注意>
以下のエゼチミブとアトルバスタチンカルシウム水和物の用法及び用量を踏まえ、患者毎に本剤の適用を考慮してください。
配合錠LD:原則として、エゼチミブ10mg及びアトルバスタチンとして10mgを併用している場合、あるいはアトルバスタチンとして10mgを使用し効果不十分な場合に、本剤LD(エゼチミブ/アトルバスタチンとして10mg/10mg)の適用を検討してください。
配合錠HD:原則として、エゼチミブ10mg及びアトルバスタチンとして20mgを併用している場合、あるいはアトルバスタチンとして2 0 m g 又はエゼチミブ/ アトルバスタチンとして10mg/10mgを使用し効果不十分な場合に、本剤HD(エゼチミブ/アトルバスタチンとして10mg/20mg)の適用を検討してください。
<効能又は効果に関連する注意>
本剤を高コレステロール血症、家族性高コレステロール血症の治療の第一選択薬として用いないでください。
<引用>
添付文書
<用法及び用量に関連する注意>
以下のエゼチミブとアトルバスタチンカルシウム水和物の用法及び用量を踏まえ、患者毎に本剤の適用を考慮してください。
配合錠LD:原則として、エゼチミブ10mg及びアトルバスタチンとして10mgを併用している場合、あるいはアトルバスタチンとして10mgを使用し効果不十分な場合に、本剤LD(エゼチミブ/アトルバスタチンとして10mg/10mg)の適用を検討してください。
配合錠HD:原則として、エゼチミブ10mg及びアトルバスタチンとして20mgを併用している場合、あるいはアトルバスタチンとして2 0 m g 又はエゼチミブ/ アトルバスタチンとして10mg/10mgを使用し効果不十分な場合に、本剤HD(エゼチミブ/アトルバスタチンとして10mg/20mg)の適用を検討してください。
<効能又は効果に関連する注意>
本剤を高コレステロール血症、家族性高コレステロール血症の治療の第一選択薬として用いないでください。
<引用>
添付文書
高齢者への投与は?
副作用の発現に注意し、副作用が発現した場合には投与を中止するなど、適切な処置を行ってください。
一般に高齢者では生理機能が低下していること、また横紋筋融解症があらわれやすいとの報告があります。
<引用>
添付文書
一般に高齢者では生理機能が低下していること、また横紋筋融解症があらわれやすいとの報告があります。
<引用>
添付文書
妊婦、授乳婦への投与は?
禁忌(次の患者には投与しないこと)
妊婦又は妊娠している可能性のある女性及び授乳婦
(「妊婦」、「授乳婦」の項参照]
妊婦又は妊娠している可能性のある女性及び授乳婦には投与しないでください。
エゼチミブとアトルバスタチンの併用投与において、ラットで胎児の発育抑制、ウサギで骨格奇形が認められています。アトルバスタチンの動物実験において、出生児数の減少及び生存、発育に対する影響が認められ、胎児にも生存率低下と発育抑制が認められています。また、ラットに他のHMG-CoA還元酵素阻害剤を大量投与した場合に胎児の骨格奇形が報告されています。更に、ヒトでは、他のHMG-CoA還元酵素阻害剤で、妊娠3ヵ月までの間に服用したとき、胎児に先天性奇形があらわれたとの報告があります。
エゼチミブでは、ヒト母乳中への移行の有無は不明ですが、妊娠後から授乳期まで投与したラットで乳児への移行が認められています。アトルバスタチンでは、ラットで乳汁中への移行が報告されています。
<引用>
添付文書
妊婦又は妊娠している可能性のある女性及び授乳婦
(「妊婦」、「授乳婦」の項参照]
妊婦又は妊娠している可能性のある女性及び授乳婦には投与しないでください。
エゼチミブとアトルバスタチンの併用投与において、ラットで胎児の発育抑制、ウサギで骨格奇形が認められています。アトルバスタチンの動物実験において、出生児数の減少及び生存、発育に対する影響が認められ、胎児にも生存率低下と発育抑制が認められています。また、ラットに他のHMG-CoA還元酵素阻害剤を大量投与した場合に胎児の骨格奇形が報告されています。更に、ヒトでは、他のHMG-CoA還元酵素阻害剤で、妊娠3ヵ月までの間に服用したとき、胎児に先天性奇形があらわれたとの報告があります。
エゼチミブでは、ヒト母乳中への移行の有無は不明ですが、妊娠後から授乳期まで投与したラットで乳児への移行が認められています。アトルバスタチンでは、ラットで乳汁中への移行が報告されています。
<引用>
添付文書
小児等への投与は?
小児等を対象とした臨床試験は実施していません。
<引用>
添付文書
<引用>
添付文書
他剤からの切替方法は?
通常、成人には1日1回1錠(エゼチミブ/アトルバスタチンとして10mg/10mg又は10mg/20mg)を食後に経口投与しますが、添付文書には次のとおり明記されていますのでご注意ください。
配合錠LD:原則として、エゼチミブ10mg及びアトルバスタチンとして10mgを併用している場合、あるいはアトルバスタチンとして10mgを使用し効果不十分な場合に、本剤LD(エゼチミブ/アトルバスタチンとして10mg/10mg)の適用を検討してください。
配合錠HD:原則として、エゼチミブ10mg及びアトルバスタチンとして20mgを併用している場合、あるいはアトルバスタチンとして2 0 m g 又はエゼチミブ/ アトルバスタチンとして10mg/10mgを使用し効果不十分な場合に、本剤HD(エゼチミブ/アトルバスタチンとして10mg/20mg)の適用を検討してください。
<引用>
添付文書
配合錠LD:原則として、エゼチミブ10mg及びアトルバスタチンとして10mgを併用している場合、あるいはアトルバスタチンとして10mgを使用し効果不十分な場合に、本剤LD(エゼチミブ/アトルバスタチンとして10mg/10mg)の適用を検討してください。
配合錠HD:原則として、エゼチミブ10mg及びアトルバスタチンとして20mgを併用している場合、あるいはアトルバスタチンとして2 0 m g 又はエゼチミブ/ アトルバスタチンとして10mg/10mgを使用し効果不十分な場合に、本剤HD(エゼチミブ/アトルバスタチンとして10mg/20mg)の適用を検討してください。
<引用>
添付文書
腎機能障害患者、透析患者への投与は?
腎機能障害患者に対して、添付文書には次のとおり明記されていますのでご注意ください。
腎障害又はその既往歴のある患者
アトルバスタチンでは横紋筋融解症の報告例の多くが腎機能障害を有する患者であり、また、横紋筋融解症に伴って急激な腎機能の悪化が認められています。
腎機能検査値異常のある患者
本剤とフィブラート系薬剤を併用する場合には、治療上やむを得ないと判断される場合にのみ併用してください。急激な腎機能悪化を伴う横紋筋融解症があらわれやすいです。
やむを得ず併用する場合には、定期的に腎機能検査等を実施し、自覚症状(筋肉痛、脱力感)の発現、CK上昇、血中及び尿中ミオグロビン上昇並びに血清クレアチニン上昇等の腎機能の悪化を認めた場合は直ちに投与を中止してください。
<引用>
添付文書
腎障害又はその既往歴のある患者
アトルバスタチンでは横紋筋融解症の報告例の多くが腎機能障害を有する患者であり、また、横紋筋融解症に伴って急激な腎機能の悪化が認められています。
腎機能検査値異常のある患者
本剤とフィブラート系薬剤を併用する場合には、治療上やむを得ないと判断される場合にのみ併用してください。急激な腎機能悪化を伴う横紋筋融解症があらわれやすいです。
やむを得ず併用する場合には、定期的に腎機能検査等を実施し、自覚症状(筋肉痛、脱力感)の発現、CK上昇、血中及び尿中ミオグロビン上昇並びに血清クレアチニン上昇等の腎機能の悪化を認めた場合は直ちに投与を中止してください。
<引用>
添付文書
肝障害患者へ投与は?
禁忌(次の患者には投与しないこと)
重篤な肝機能障害のある患者及び肝代謝能が低下していると考えられる以下のような患者
急性肝炎、慢性肝炎の急性増悪、肝硬変、肝癌、黄疸
(「重篤な肝機能障害のある患者及び肝代謝能が低下していると考えられる以下のような患者」、「肝機能障害患者」の項参照)
肝機能障害患者に対する使用上の注意として、添付文書には次のとおり明記されていますのでご注意ください。
重篤な肝機能障害のある患者及び肝代謝能が低下していると考えられる以下のような患者(急性肝炎、慢性肝炎の急性増悪、肝硬変、肝癌、黄疸)には投与しないでください。
アトルバスタチンの血漿中濃度が上昇し、副作用の発現頻度が増加するおそれがあります。また、アトルバスタチンは主に肝臓において作用し代謝されるので、肝障害を悪化させるおそれがあります。
中等度の肝機能障害のある患者
投与しないことが望ましいです。エゼチミブの血漿中濃度が上昇するおそれがあります。
肝障害又はその既往歴のある患者
エゼチミブでは肝機能障害の程度に応じて血漿中薬物濃度の上昇が認められました。アトルバスタチンは主に肝臓において作用し代謝されるので、肝障害を悪化させるおそれがあります。
<引用>
添付文書
重篤な肝機能障害のある患者及び肝代謝能が低下していると考えられる以下のような患者
急性肝炎、慢性肝炎の急性増悪、肝硬変、肝癌、黄疸
(「重篤な肝機能障害のある患者及び肝代謝能が低下していると考えられる以下のような患者」、「肝機能障害患者」の項参照)
肝機能障害患者に対する使用上の注意として、添付文書には次のとおり明記されていますのでご注意ください。
重篤な肝機能障害のある患者及び肝代謝能が低下していると考えられる以下のような患者(急性肝炎、慢性肝炎の急性増悪、肝硬変、肝癌、黄疸)には投与しないでください。
アトルバスタチンの血漿中濃度が上昇し、副作用の発現頻度が増加するおそれがあります。また、アトルバスタチンは主に肝臓において作用し代謝されるので、肝障害を悪化させるおそれがあります。
中等度の肝機能障害のある患者
投与しないことが望ましいです。エゼチミブの血漿中濃度が上昇するおそれがあります。
肝障害又はその既往歴のある患者
エゼチミブでは肝機能障害の程度に応じて血漿中薬物濃度の上昇が認められました。アトルバスタチンは主に肝臓において作用し代謝されるので、肝障害を悪化させるおそれがあります。
<引用>
添付文書
粉砕して投与できますか?
【適応外】
本剤を粉砕して投与することは、承認外の用法となります。
粉砕して投与した際の薬物動態、有効性、安全性は検討していませんので、おすすめしていません。
光及び酸化を避けるため、PTPシートのまま保存し、服用直前にPTPシートから取り出してください。
<引用>
添付文書
<参考>
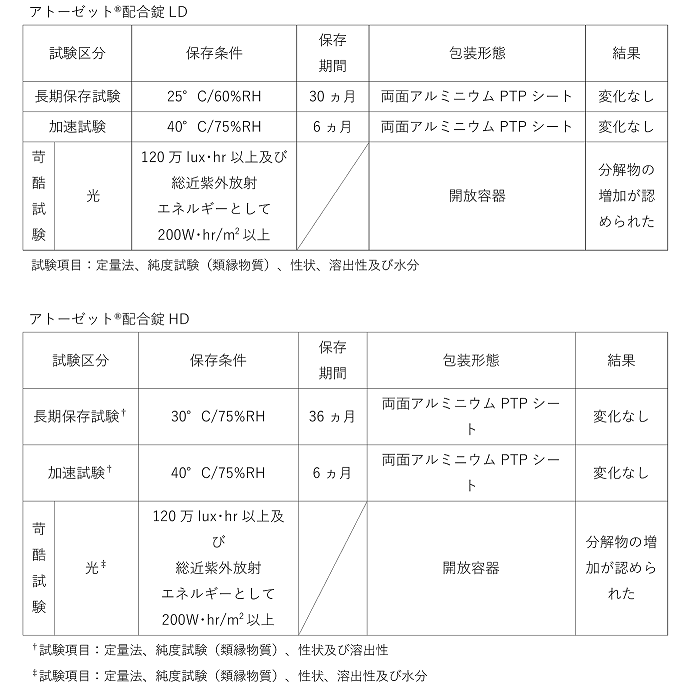
本剤を粉砕して投与することは、承認外の用法となります。
粉砕して投与した際の薬物動態、有効性、安全性は検討していませんので、おすすめしていません。
光及び酸化を避けるため、PTPシートのまま保存し、服用直前にPTPシートから取り出してください。
<引用>
添付文書
<参考>

簡易懸濁して投与できますか?
【適応外】
本剤を簡易懸濁して投与することは、承認外の用法となります。
簡易懸濁して投与した際の薬物動態、有効性、安全性は検討していませんので、おすすめしていません。
光及び酸化を避けるため、PTPシートのまま保存し、服用直前にPTPシートから取り出してください。
<引用>
添付文書
<参考>

本剤を簡易懸濁して投与することは、承認外の用法となります。
簡易懸濁して投与した際の薬物動態、有効性、安全性は検討していませんので、おすすめしていません。
光及び酸化を避けるため、PTPシートのまま保存し、服用直前にPTPシートから取り出してください。
<引用>
添付文書
<参考>

錠剤を分割して投与できますか?
【適応外】
本剤を分割して投与することは、承認外の⽤法となります。
分割後の安定性について検討していませんので、おすすめしていません。
光及び酸化を避けるため、PTPシートのまま保存し、服用直前にPTPシートから取り出してください。
<引用>
添付文書
<参考>

本剤を分割して投与することは、承認外の⽤法となります。
分割後の安定性について検討していませんので、おすすめしていません。
光及び酸化を避けるため、PTPシートのまま保存し、服用直前にPTPシートから取り出してください。
<引用>
添付文書
<参考>

分包・一包化はできますか?
本剤を分包又は他剤と一包化した際の安定性について検討していませんので、おすすめしていません。
光及び酸化を避けるため、PTPシートのまま保存し、服用直前にPTPシートから取り出してください。
<引用>
添付文書
<参考>

光及び酸化を避けるため、PTPシートのまま保存し、服用直前にPTPシートから取り出してください。
<引用>
添付文書
<参考>

安全性
主な副作用は?
重大な副作用(頻度不明)として、過敏症、中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、多形紅斑、横紋筋融解症、ミオパチー、免疫介在性壊死性ミオパチー、劇症肝炎、肝炎、肝機能障害、黄疸、無顆粒球症、汎血球減少症、血小板減少症、高血糖、糖尿病、間質性肺炎が報告されています。
その他の副作用として、ALT増加(1%以上)、胃炎、腹部膨満、便秘、AST増加、γ-GTP増加、Al-P増加(以上1%未満)、結膜炎、口腔ヘルペス、帯状疱疹、インフルエンザ、肺炎、悪夢、睡眠障害、不眠(症)、うつ病、抑うつ、めまい、しびれ、頭痛、異常感覚、錯感覚、味覚異常、眠気、健忘症、脳梗塞、坐骨神経痛、末梢性ニューロパチー、期外収縮、動悸、頻脈、洞性徐脈、咳嗽、呼吸困難、悪心、嘔吐、消化不良、腹痛、下痢、膵炎、口唇炎、口内炎、口内乾燥、口腔内不快感、口のしびれ、舌のしびれ、舌炎、舌痛、胸やけ、胃食道逆流性疾患、胃不快感、心窩部痛(心窩部の疼痛)、鼓腸放屁、腹部不快感、下腹部痛、軟便、排便回数増加、胆汁うっ滞性黄疸、胆石症、胆嚢炎、そう痒症、発疹、ざ瘡、蕁麻疹、発赤、光線過敏、皮膚乾燥、皮膚亀裂、脱毛症、爪の障害、関節痛、筋肉痛、筋痙縮、背部痛、頸・肩のこり、こわばり感、四肢痛、筋肉疲労、筋力低下、筋炎、腱炎、腱痛、蛋白尿、血尿、着色尿、排尿困難、頻尿、胸痛、無力症、浮腫(顔面・四肢等)、口渇、疼痛、熱感、発熱、全身倦󠄁怠(感)、疲労、血中CK増加、BUN増加、HbA1c増加、アミラーゼ増加、肝機能検査異常、血圧上昇、血小板数減少、血中ACTH増加、血中K増加、血中LDH増加、血中TSH増加、血中アルドステロン減少、血中クレアチニン増加、血中コリンエステラーゼ増加、血中コルチゾール増加、血中テストステロン減少、血中ビリルビン増加、血中ブドウ糖増加、血中ミオグロビン増加、血中リン増加、血中鉄減少、血中尿酸増加、体重増加、白血球数減少、食欲減退、耳鳴、霧視、ほてり、貧血、低血糖、女性化乳房、勃起不全(以上頻度不明)が報告されています。
安全性情報については添付文書の副作用及び臨床成績の安全性の結果をご参照ください。
その他の副作用として、ALT増加(1%以上)、胃炎、腹部膨満、便秘、AST増加、γ-GTP増加、Al-P増加(以上1%未満)、結膜炎、口腔ヘルペス、帯状疱疹、インフルエンザ、肺炎、悪夢、睡眠障害、不眠(症)、うつ病、抑うつ、めまい、しびれ、頭痛、異常感覚、錯感覚、味覚異常、眠気、健忘症、脳梗塞、坐骨神経痛、末梢性ニューロパチー、期外収縮、動悸、頻脈、洞性徐脈、咳嗽、呼吸困難、悪心、嘔吐、消化不良、腹痛、下痢、膵炎、口唇炎、口内炎、口内乾燥、口腔内不快感、口のしびれ、舌のしびれ、舌炎、舌痛、胸やけ、胃食道逆流性疾患、胃不快感、心窩部痛(心窩部の疼痛)、鼓腸放屁、腹部不快感、下腹部痛、軟便、排便回数増加、胆汁うっ滞性黄疸、胆石症、胆嚢炎、そう痒症、発疹、ざ瘡、蕁麻疹、発赤、光線過敏、皮膚乾燥、皮膚亀裂、脱毛症、爪の障害、関節痛、筋肉痛、筋痙縮、背部痛、頸・肩のこり、こわばり感、四肢痛、筋肉疲労、筋力低下、筋炎、腱炎、腱痛、蛋白尿、血尿、着色尿、排尿困難、頻尿、胸痛、無力症、浮腫(顔面・四肢等)、口渇、疼痛、熱感、発熱、全身倦󠄁怠(感)、疲労、血中CK増加、BUN増加、HbA1c増加、アミラーゼ増加、肝機能検査異常、血圧上昇、血小板数減少、血中ACTH増加、血中K増加、血中LDH増加、血中TSH増加、血中アルドステロン減少、血中クレアチニン増加、血中コリンエステラーゼ増加、血中コルチゾール増加、血中テストステロン減少、血中ビリルビン増加、血中ブドウ糖増加、血中ミオグロビン増加、血中リン増加、血中鉄減少、血中尿酸増加、体重増加、白血球数減少、食欲減退、耳鳴、霧視、ほてり、貧血、低血糖、女性化乳房、勃起不全(以上頻度不明)が報告されています。
安全性情報については添付文書の副作用及び臨床成績の安全性の結果をご参照ください。
